Konnatale Fehlbildungen
Einleitung
Durch Störungen in der Embryonalentwicklung können verschiedenste Fehlbildungen beim Neugeborenen auftreten. Exemplarisch sollen hier die hypertrophe Pylorusstenose sowie die Ösophagusatresie behandelt werden.
Hypertrophe Pylorusstenose
Bei diesem Krankheitsbild handelt es sich um eine funktionelle Entleerungsstörung des Magens, die bedingt wird durch die fehlende Relaxation des Pylorus am Magenausgang. Die ringförmige Muskulatur ist in diesem Bereich verdickt, was letztlich die Stenose erzeugt.
Die typische Klinik tritt in den ersten Lebenswochen auf und ist geprägt durch schwallartiges Erbrechen von nicht galligem Mageninhalt sowie Gedeihstörungen trotz gutem Trinkverhaltens. In der Regel kommt es unmittelbar nach Nahrungsaufnahme zu starkem Erbrechen. Mitunter ist die im Magen vorhandene Hyperperistaltik durch die Bauchdecke zu sehen bzw. zu palpieren.
Diagnostik
Die Diagnosestellung gelingt in der Regel sonografisch. Hier kann die verdickte Pylorusmuskulatur identifiziert und ausgemessen werden. Ist die Länge des Pylorus länger als 14 mm und die Magenwand in diesem Bereich dicker als 3 mm gilt die Diagnose als gesichert.1Auf weiterführende Diagnostik wie z.B. eine Röntgenuntersuchung mit Kontrastmittel kann auf Grund der hohen Sensitivität und Spezifität der Sonografie in den allermeisten Fällen verzichtet werden.2
Therapie
Durch das weiderholte Erbrechen von saurem Mageninhalt kommt es zu einer Elektrolytverschiebung im Sinne einer metabolischen Alkalose, die es durch Infusionstherapie auszugleichen gilt. Darüber hinaus besteht die erste Maßnahme zur Behandlung der hypertrophen Pylorusstenose in der Ableitung über eine nasogastrale Sonde.
Die definitive Therapie besteht in einer chirurgischen Durchtrennung der hypertrophen Pylorusmuskulatur. Auf Grund der exzellenten Ergebnisse dieser operativen Maßnahme spielen konservative Behandlungsmöglichkeiten bei diesem Krankheitsbild keine entscheidende Rolle.
Operation
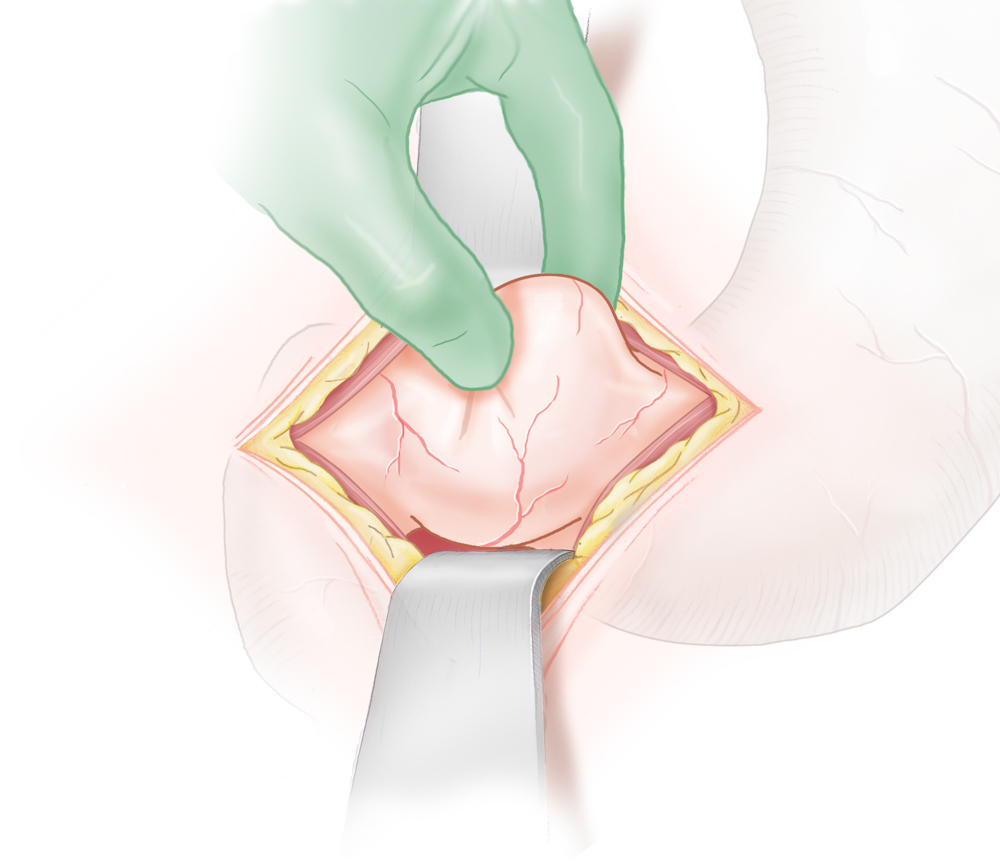
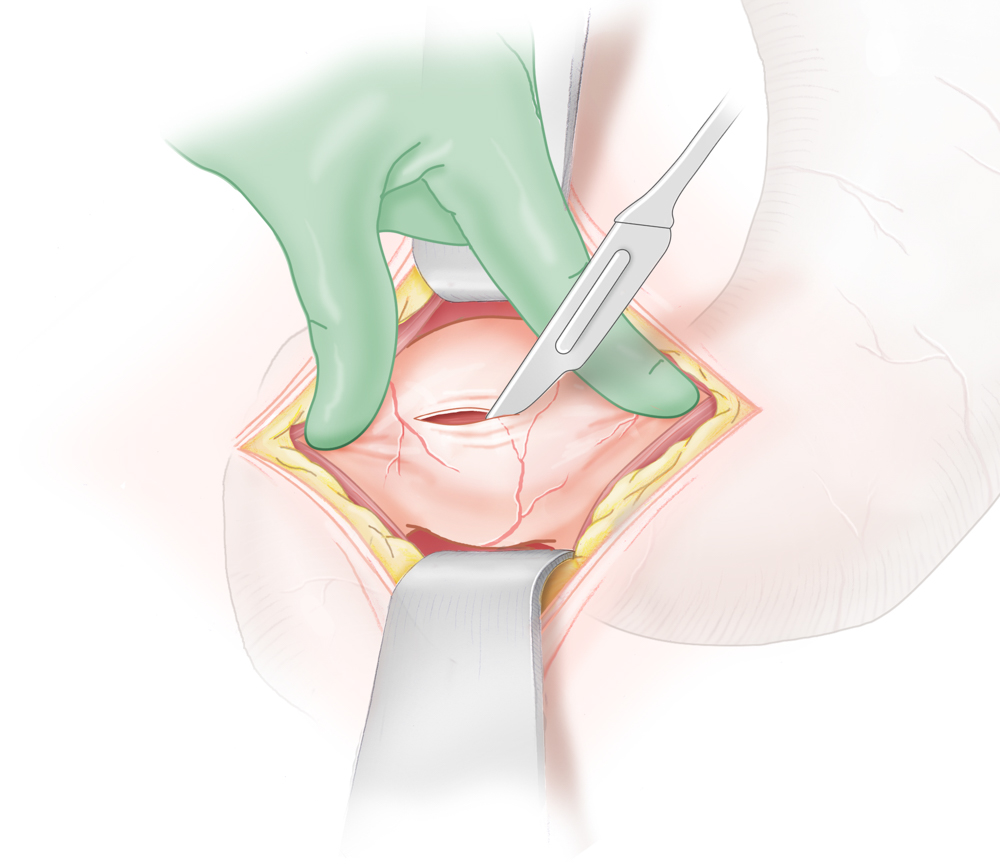
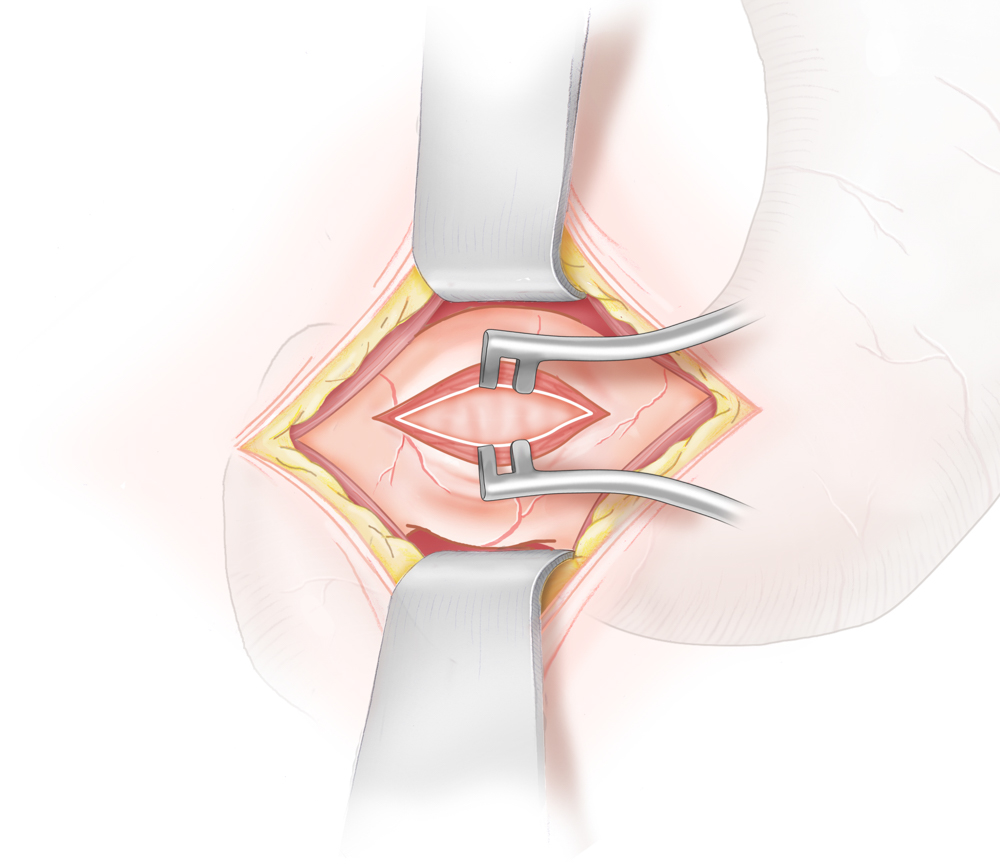
Die von Ramsted 1912 eingeführte Pyloromyotomie stellt in modifizierter Form (Weber-Ramsted-OP) nach wie vor das Standard-Operationsverfahren dar. Hierbei wird der Pylorus über einen supraumbilicalen Schnitt vor die Bauchdecke verlagert freigelegt. Auf der gesamten Länge wird die Serosa inzidiert und die darunterliegende Muskulatur mit einem Klemmchen gespreizt, bis die Mukosa freiliegt. Auch minimalinvasive Techniken wurden entwickelt, bei der die Pyloromyotomie laparoskopisch durchgeführt wird.
In ca. 5% der Fälle kommt es zu einer akzidentiellen Eröffnung der Mukosa.3Diese wird dann mit einem resorbierbaren Nahtmaterial übernäht und ggf. mit einer Omentumplastik gedeckt. Auch kann es zu einer inkompletten Myotomie kommen, hier ist die Rate mit 5,5% bei den endoskopischen Verfahren höher als bei der offenen Operationstechnik (ca. 2%). Der Vorteil der laparoskopischen Verfahren liegt neben des offensichtlich etwas besseren kosmetischen Ergebnis vor allem in der Reduktion der postoperativen Schmerzen. Die dadurch ermöglichte Reduktion der Schmerzmittelgabe bedingt einen schnelleren Kostaufbau. Auch der Krankenhausaufenthalt ist nach laparoskopischen Verfahren in der Regel kürzer.4-6
Ösophagusatresie
Da sich der Ösophagus und das Tracheobronchialsystem in der embryologischen Entwicklung gemeinsam aus dem Vorderdarm bildet, kommt es bei Fehlbildung in diesem Bereich häufig zu Fistelbildungen zwischen Ösophagus und Trachea bzw. den Bronchien.
Anatomisch lässt sich der Ösophagus in eine pars cervicalis, pars thoracalis sowie pars abdominalis einteilen. Auf ihrem Weg ins Abdomen weist die Speiseröhre drei Engstellen auf: der oberer Ösophagussphinkter, die Passagestelle der Aorta ascendens sowie den Durchtritt durch das Zwerchfell. Dies sind die Prädileketionsstellen für Perforationen, Fremdkörperimpaktationen sowie funktionelle Erkrankungen und Divertikel. All diese Krankheitsbilder werden an anderer Stelle besprochen.
Klassifikation
Kommt es in der Embryonalentwicklung zu einer unvollständigen Separation von Speiseröhre und Tracheobronchialsystem. Je nach Ausprägung sind unterschiedliche Fistelverbindungen zwischen den beiden Organsystemen möglich.
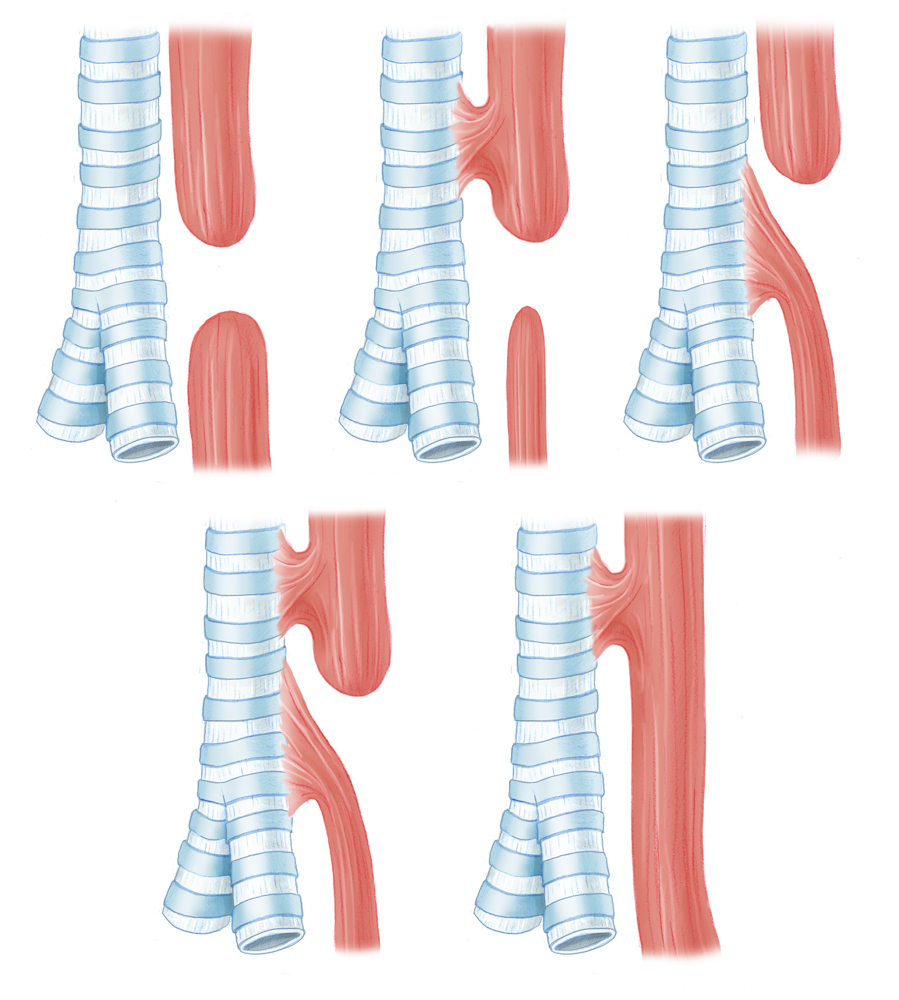
Die Einteilung nach Vogt unterscheidet 3 Haupttypen. Im englischen Sprachgebrauch ist die Klassifikation nach Gross geläufiger, der dieselben Einteilungsprinzipien zu Grunde liegen.
Die häufigste Form ist mit 90% die Unterform 3b nach Vogt, bei der der proximale Ösophagus blind endet und der distale Stumpf eine Verbindung zur Trachealbifurkation aufweist. Die Typen Vogt 2 sowie Vogt 4 sind mit 5% bzw. 2-4% deutlich seltener. Alle übrigen Formen stellen eine Rarität dar.
Diagnostik
Sonografisch kann während der Schwangerschaft eine fehlende Magenblase bzw. das Vorliegen eines erweiterten aber blind endenden Ösophagus hinweisend sein auf das Vorliegen einer Ösophagusatresie. Zusätzlich liegt zumeist ein Polyhydramnion vor. Häufig wird die Diagnose aber nicht präpartal gestellt.
Postpartal fällt das Neugeborene durch Zeichen der Aspiration auf bzw. durch vermehrtes schaumiges Speicheln. Liegt eine distale Verbindung von Ösophagus und Tracheobronchialsystem vor, kann eine Überblähung des Gastrointestinaltraktes klinisch evident und auf einer Röntgenaufnahme sichtbar werden.
Beim – vorsichtigen – Vorschieben einer Magensonde ergibt sich ein federnder Widerstand, was die Verdachtsdiagnose weiter erhärtet. Zur definitiven Diagnostik der Ösophagusatresie wird ein Röntgenbild des Thorax sowie des Abdomens bei liegender Magensonde durchgeführt. Damit wird das untere Ende des blind endenden Ösophagus visualisiert. Sind Magen und Darm nicht mit Luft gefüllt, macht dies das Vorliegen einer distalen Fistel unwahrscheinlich. Die Verwendung von wasserlöslichem Kontrastmittel ist nur in Ausnahmefällen erforderlich.
Begleitende Fehlbildungen vor allem des Herzens und der thorakalen Aorta sollten parallel ausgeschlossen werden.
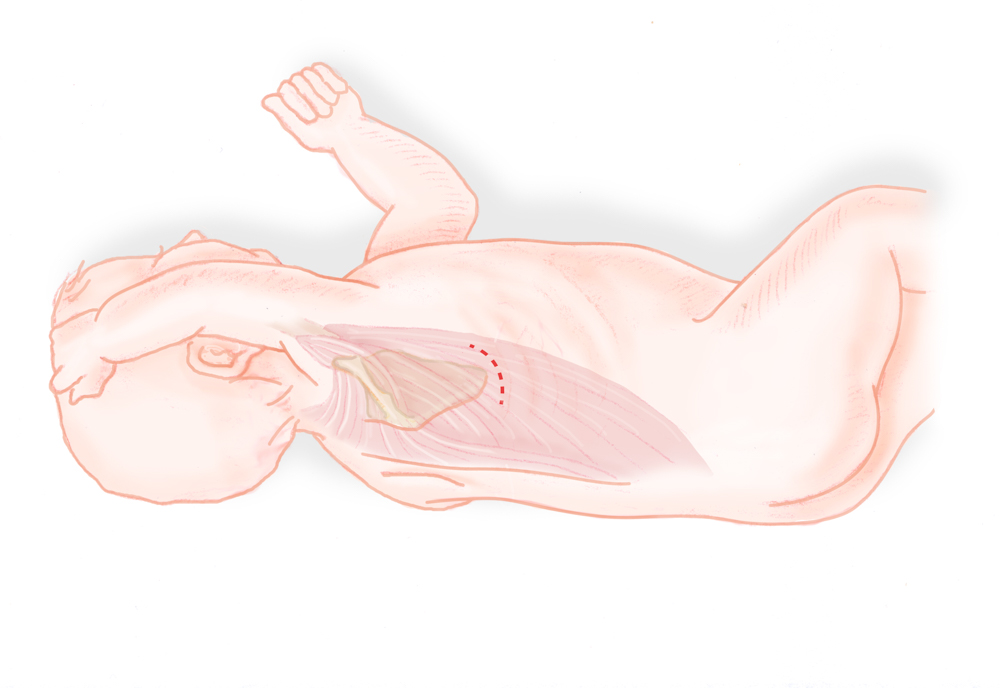
Therapie
Bei kardiopulmonal stabilem Neugeborenen erfolgt die operative Versorgung in den ersten 24 Lebensstunden. Nur bei einer massiven Überblähung des Magens mit der Gefahr der Minderperfusion oder gar Ruptur auf dem Boden einer distalen Fistel besteht die Indikation zur notfallmäßigen Versorgung.
Bei der operativen Versorgung wird stets versucht, den Ösophagus zu erhalten. Die Fistel wird ligiert und die Kontinuität der Speiseröhre durch Anastomosierung hergestellt. Die offene Operation erfolgt über einen rechtsthorakalen Zugang. Der Säugling wird dabei auf die linke Seite gelagert. Unter Durchtrennung der Interkostalmuskulatur wird in den Thorax eingegangen, die Lunge kollabiert dank einer Doppellumenintubation, so dass der Zugang zum Ösophagus möglich wird. In Einzelfällen kann die Durchtrennung der V. azygos notwendig werden, allerdings scheint dies mit einer höheren Rate an postoperativen pulmonalen Komplikationen vergesellschaftet zu sein sowie das Risiko einer Anastomoseninsuffizienz zu erhöhen.7
Als postoperative Komplikationen drohen eine Anastomoseninsuffizienz mit konsekutiver Mediastinitis und Sepsis sowie langfristig eine Anastomosenstenose. Letztere kann in der Regel endoskopisch durch wiederholte Bougierungen oder Stenteinlagen behandelt werden. Eine Anastomoseninsuffizenz zwingt meistens zu einer operativen Revision, wobei endoskopisch eingebrachte Vakuum-Schwammsysteme (EndoVac) zunehmend gute Erfolge zeigen bei Leckagen in der Ösophaguschirurgie.8Tritt ein Rezidiv der Fistel auf, so ist dies häufig Folge eine Anastomosenleckage.
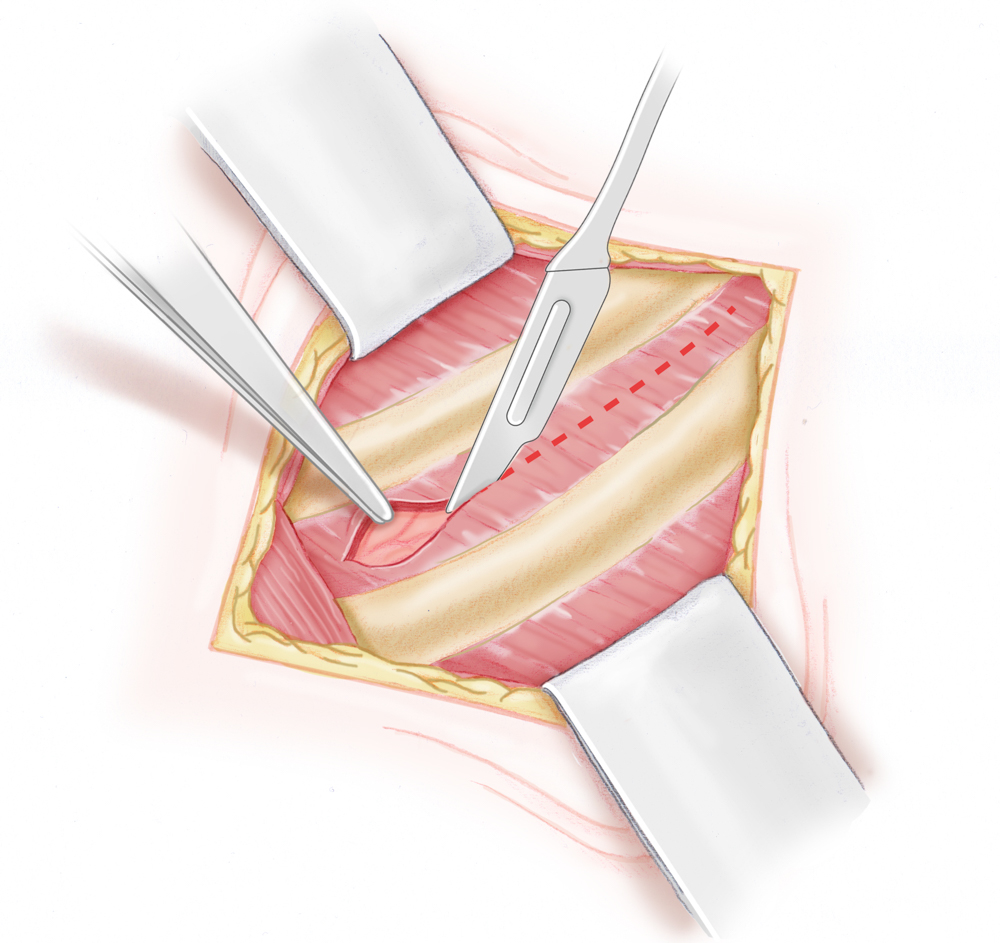
Thorakotomie
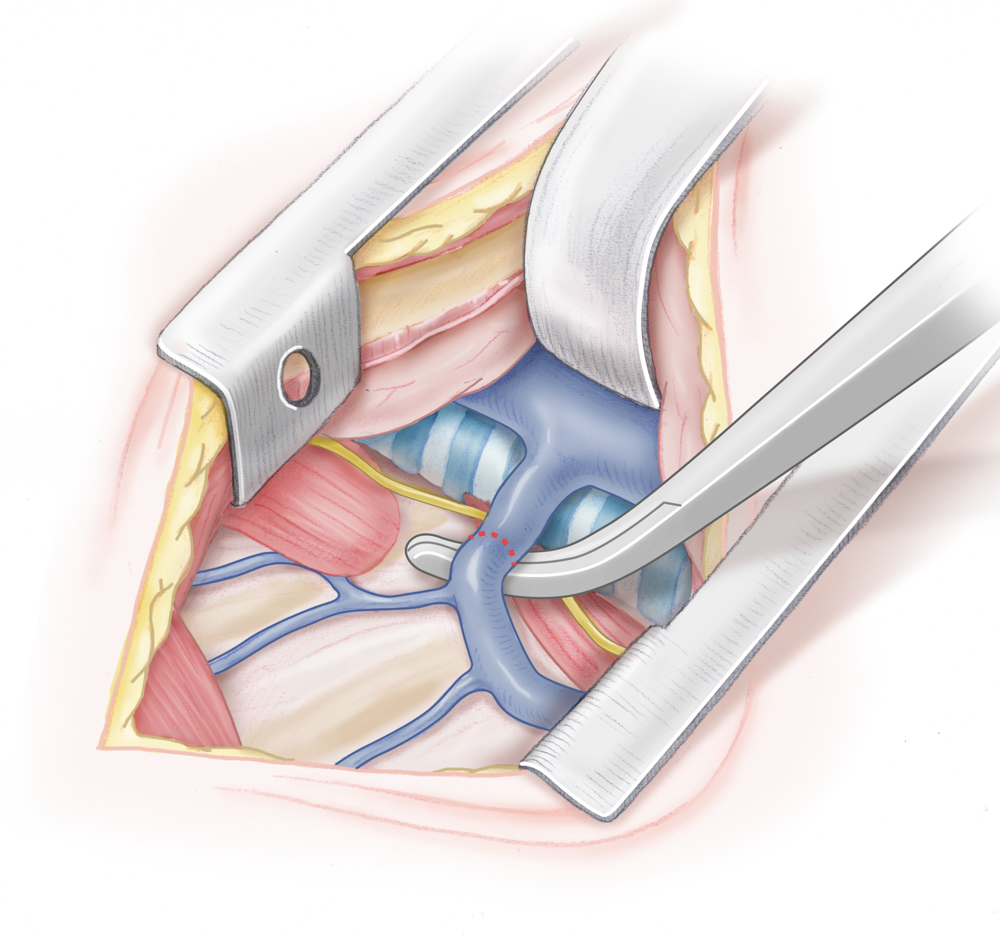
Liagtur der V. azygos
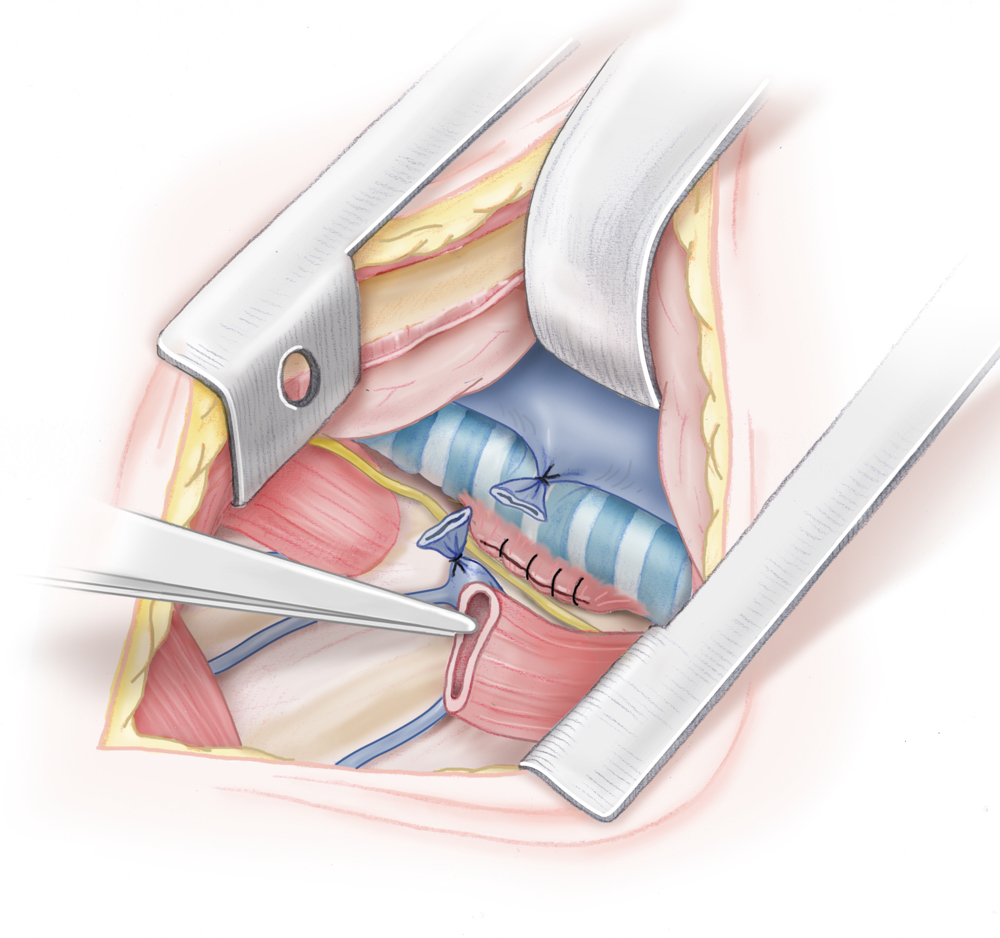
Anastomosierung des Ösophagus
Literatur
- Aspelund G, Langer JC. Current management of hypertrophic pyloric stenosis. Semin Pediatr Surg. 2007;16(1):27-33.
- White MC, Langer JC, Don S, DeBaun MR. Sensitivity and cost minimization analysis of radiology versus olive palpation for the diagnosis of hypertrophic pyloric stenosis. J Pediatr Surg. 1998;33(6):913-917.
- Hulka F, Harrison MW, Campbell TJ, Campbell JR. Complications of pyloromyotomy for infantile hypertrophic pyloric stenosis. Am J Surg. 1997;173(5):450-452.
- Leclair MD, Plattner V, Mirallie E, et al. Laparoscopic pyloromyotomy for hypertrophic pyloric stenosis: a prospective, randomized controlled trial. J Pediatr Surg. 2007;42(4):692-698.
- St Peter SD, Holcomb GW, 3rd, Calkins CM, et al. Open versus laparoscopic pyloromyotomy for pyloric stenosis: a prospective, randomized trial. Annals of surgery. 2006;244(3):363-370.
- Oomen MW, Hoekstra LT, Bakx R, Ubbink DT, Heij HA. Open versus laparoscopic pyloromyotomy for hypertrophic pyloric stenosis: a systematic review and meta-analysis focusing on major complications. Surgical endoscopy. 2012;26(8):2104-2110.
- Upadhyaya VD, Gangopadhyaya AN, Gopal SC, et al. Is ligation of azygos vein necessary in primary repair of tracheoesophageal fistula with esophageal atresia? Eur J Pediatr Surg. 2007;17(4):236-240.
- Goenka MK, Goenka U. Endotherapy of leaks and fistula. World J Gastrointest Endosc. 2015;7(7):702-713.
