Aneurysma der descendierenden thorakalen Aorta (DTAA) und Thorako-abdominelles Aortenaneurysma (TAAA)
Als thorako-abdominelles Aortenaneurysma bezeichnet man die gleichzeitige aneurysmatische Erweiterung von thorakaler und abdomineller Aorta, wobei der Aortendurchmesser dabei auf das über 1,5 Fache angewachsen ist.
Hauptsächlich handelt es sich dabei um degenerative Aneurysmen, in ca. 15-20% der Fälle geht eine Dissektion voraus. Eine zugrundeliegende Bindegewebs- oder Texturstörung (Marfan-/Ehlers-Danlos-/Loeys-Dietz-Syndrom) ist möglich. Seltener sind Traumen oder entzündliche/infektiöse Gefäßprozesse die Ursache.
Meistens asymptomatisch und als Zufallsbefund bei CT/MRT oder Ultraschall entdeckt, verursachen symptomatische Aneurysmen oft unspezifische Beschwerden in Brust, Rücken, Flanke oder Bauch.
Die Einteilung nach Crawford, mod. nach Safi unterscheidet fünf Typen (aus Cronenwett JL, Johnston W (eds) (2010) Rutherford`s Vascular Surgery, 8. Aufl. Elsevier, Philadelphia). Hier werden die Aneurysmen der descendierenden thorakalen Aorta (DTAA) mit denen der thorako-abdominellen Aorta (TAAA) in ihrer Einteilung kombiniert:
Typ I : Ausbreitung von der linken Arteria subclavia bis zum renoviszeralen Segment
Typ II :Ausbreitung von der linken Arteria subclavia bis zur Iliacalbifurkation
Typ III : Ausbreitung von der Aorta decendens in Höhe Th 6 bis zur Iliacalbifurkation
Typ IV :Ausbreitunginfradiaphragmal renoviszeral bis zur Iliacalbifurkation
Typ V : Ausbreitungvon der Aorta descendens in Höhe Th 6 bis zum renoviszeralen Segment
Klassifikation der thorakalen
Aortenaneurysmen nach Safi
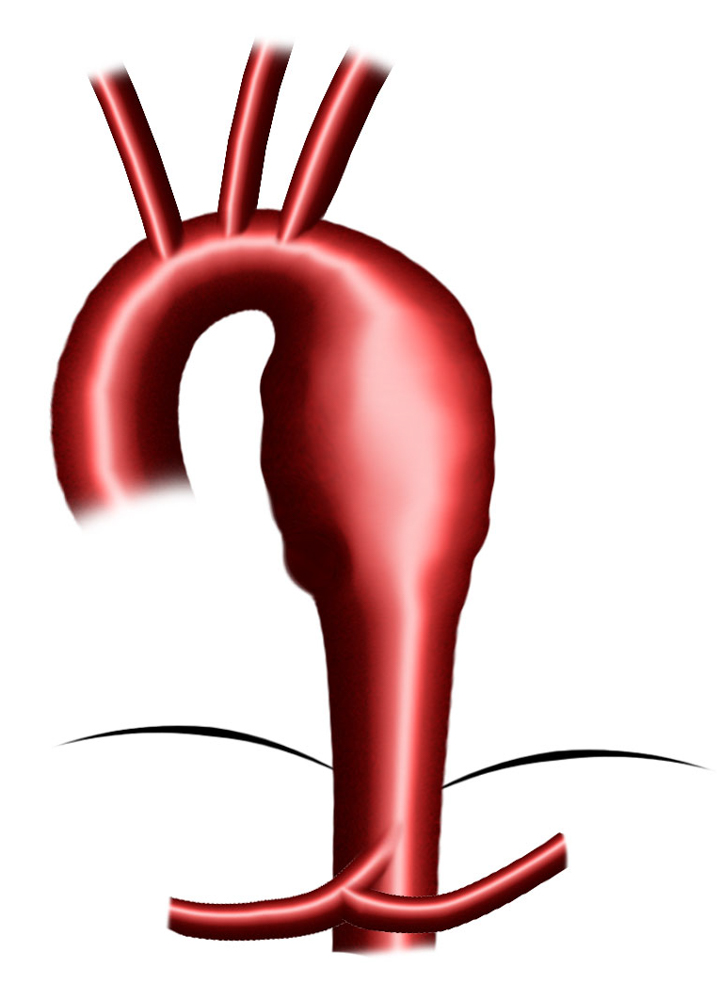 Typ A
Typ A
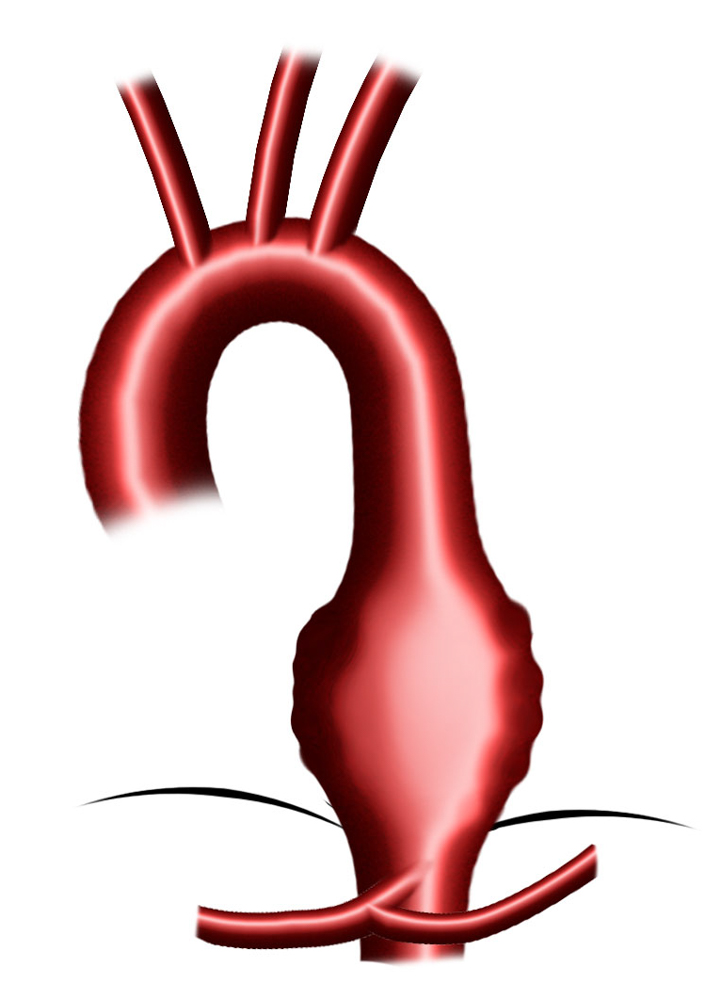 Typ B
Typ B
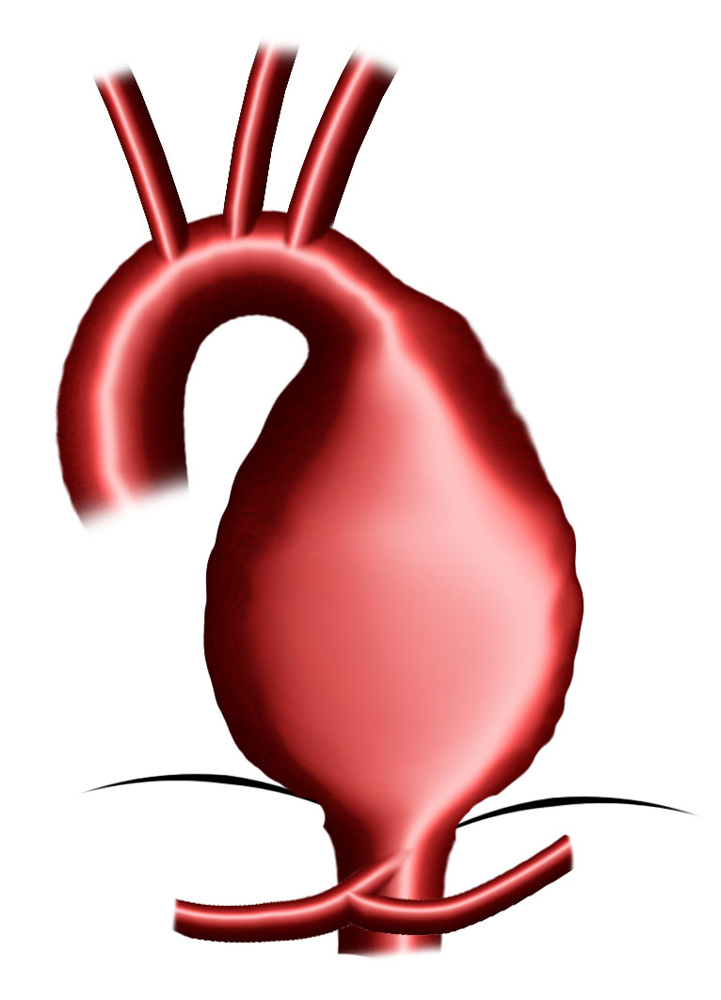 Typ C
Typ C
Klassifikation der thorakoabdominalen
Aortenaneurysmen nach Crawford
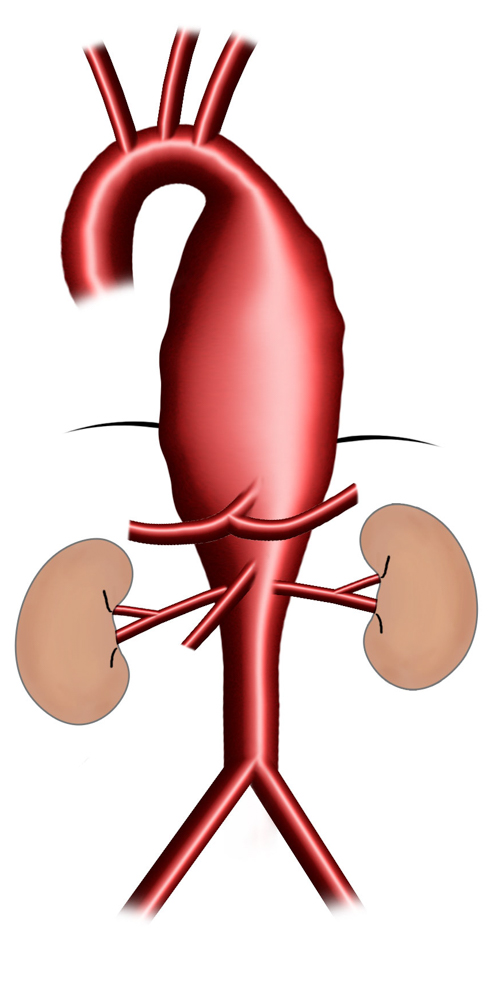
Typ I
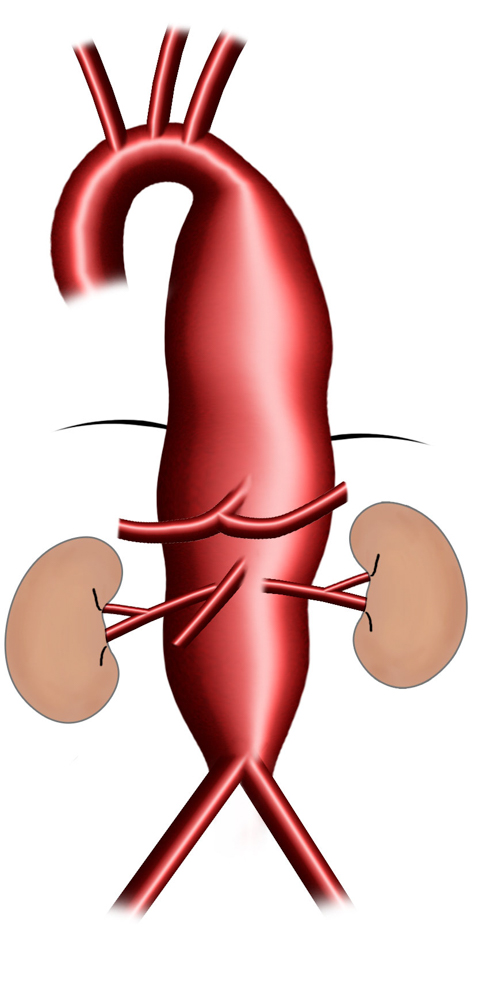
Typ II
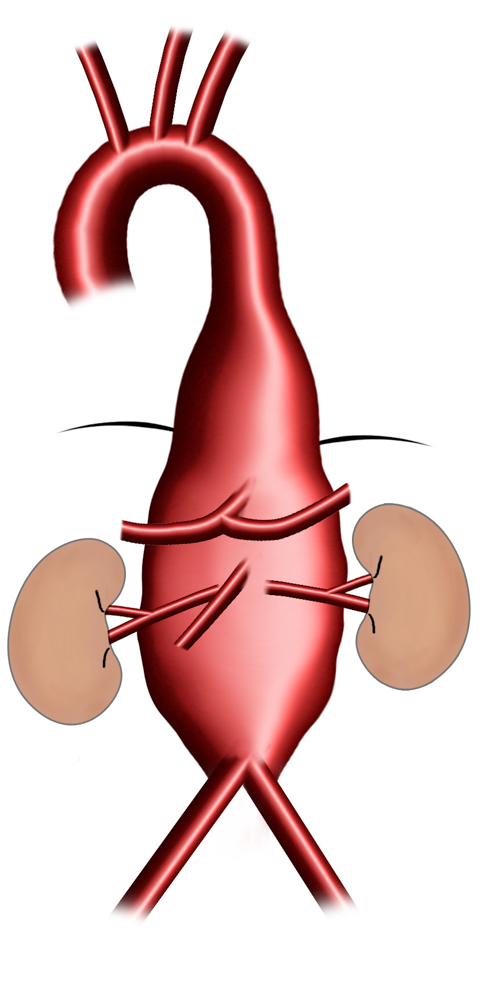
Typ III
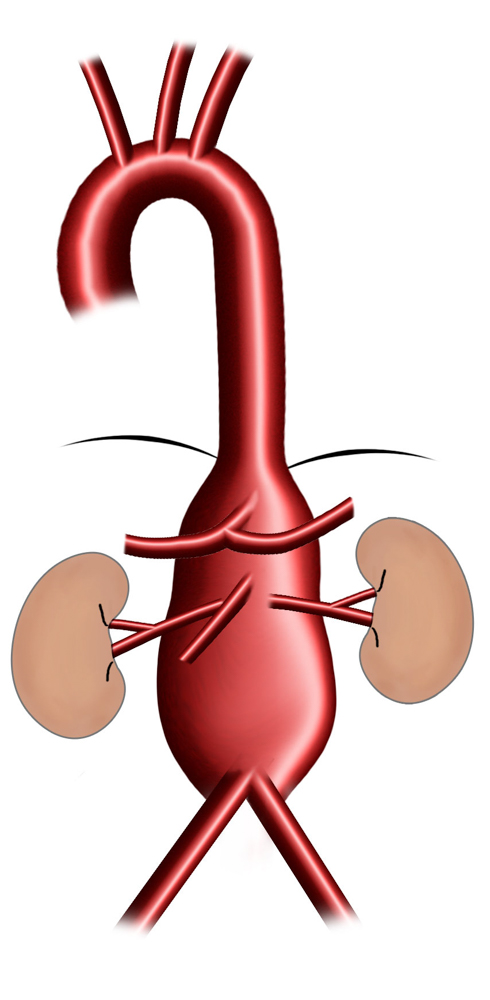
Typ IV
Diagnostik
Für die Diagnosestellung und Planung der heutzutage meist endovasculären Therapie ist die Durchführung einer Dünnschicht CT-Angiographie von thorakaler und abdomineller Aorta in 1mm-Schnitten essentiell.
Eine Therapieindikation wird beim asymptomatischen TAAA ohne Texturstörung ab 6cm Durchmesser bzw. 0,5cm Wachstumsrate/Jahr gesehen, bei Vorliegen einer zugrundeliegenden Bindegewebserkrankung ab 5cm Durchmesser (Koeppel TA, Greiner A, Jacobs MJ (2010) DGG-Leitlinie: Thorakale und thorakoabdominelle Aortenaneurysmen. http://www.gefaesschirurgie.de/fileadmin/websites/dgg/downloads/LL_DTAA_undTAAA_2011.pdf).
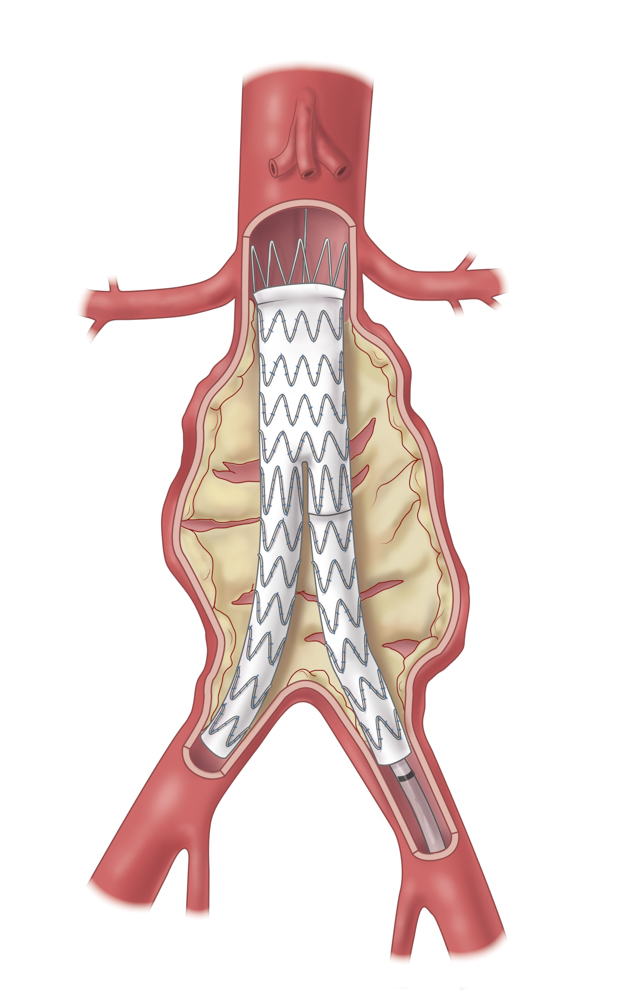
Therapie
Sofern keine Texturstörung vorliegt, erfolgt die Ausschaltung eines TAAAs heute standardmäßig endovasculär über die Einbringung von aortalen Stentgrafts (ummantelten Stentprothesen) als sogenannte TEVAR (Thoracic EndoVascular Aortic Repair). Mittlerweile ist es möglich, das renoviszerale Segment (Segment IV der Aorta nach Ishimaru) mithilfe spezieller gefensterter/fenestrierter Gefäßprothesen oder Prothesen mit Seitenarmen/branches zu versorgen. So können nach CT-Vordiagnostik mittlerweile sogenannte 4fach gebranchte Prothesen als custom-made-devices vorgefertigt und in das Segment IV der Aorta implantiert werden.
Durch zusätzliche gecoverte Stents können ferner Schornstein- („chimney“), Periskop- („periscope“) oder Schnorchel- („snorkel“) Konfigurationen geschaffen werden und so Landungs- und Verankerungszonen für Standard-Stentprothesen künstlich geschaffen werden (siehe Kapitel BAA).
Eine Kombination von Stentprozedur und offener Operation im Sinne von Hybridoperationen ist ebenfalls möglich (z.b. Tube-stent + viszerales Debranching im Sinne einer „Oktopus-Operation“) und kann in Einzelfällen notwendig sein, wenn eine rein endovasculäre Behandlung nicht möglich ist.
Eine Alternative stellt insbesondere bei Texturstörungen und jungen, fitten Patienten mit hoher Lebenserwartung der offene Aortenersatz mit dem OP-Zugang nach Crawford dar.
Die „Achillesferse“ der offenen und endovasculären Versorgung thorako-abdomineller Aortenaneurysmen bleibt die Kompromittierung der Rückenmarksdurchblutung durch den langstreckigen Aortenersatz mit dem gefürchteten klinischen Bild der „Spinalen Ischämie“ (Paraparese/plegie, Blasen- und Mastdarmstörung).
Mittlerweile wird davon ausgegangen, dass die Rückenmarksdurchblutung anstatt über eine einzelne Arterie (veraltete Ansicht: A. radicularis magna) über einen multisegmentalen Zufluss erfolgt und hier insbesondere die linke Arteria subclavia und die Arteria iliaca interna eine wichtige Rolle spielen.
Verschiedene Therapiestrategien und -Ansätze sollen der Ausbildung einer spinalen Ischämie nach und bei der Versorgung eines DTAAs/TAAAs vorbeugen: zweizeitige Versorgung von thorakalem und abdominellem Aneurysma-Anteil, Liquordrainage, um Spinaldruck < 10mmHg ablassen zu können, Anheben des mittleren arteriellen Drucks (MAD) >85mmHg, Offenlassen von Prothesenseitenarmen sowie diverse Neuromonitoringverfahren.
Auch trotz Protektion kann das Risiko für eine spinale Ischämie bei der Versorgung eines thorako-abdominellen Aneurysmas jedoch noch bis zu 23% betragen (Dias NV, Sonesson B, Kristmundsson T, Holm H, Resch T (2015) Shortterm outcome of spinal cord ischemia after andovascular repair of thoracoabdominal aortic aneurysms. Eur J Vasc Endovasc Surg 49: 403-409).

