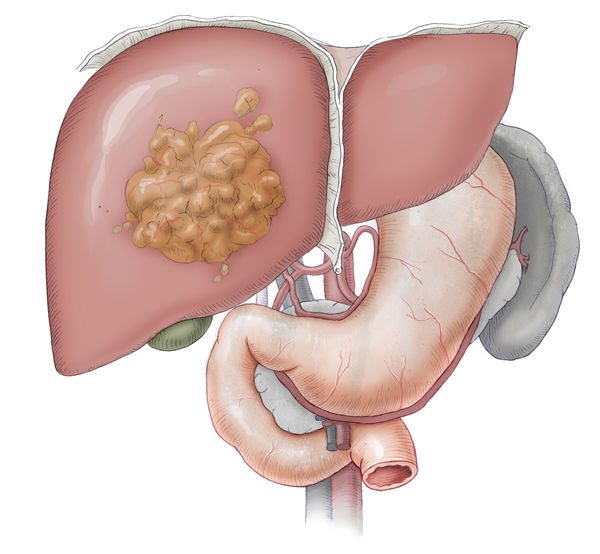
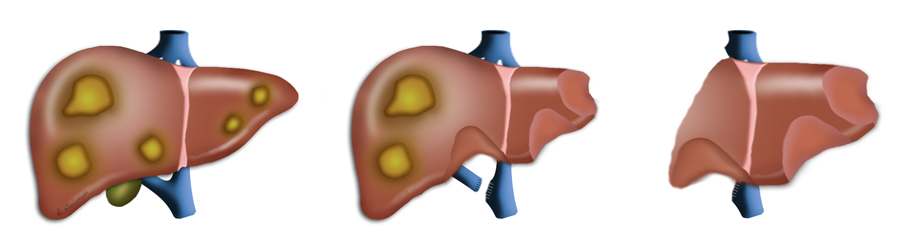
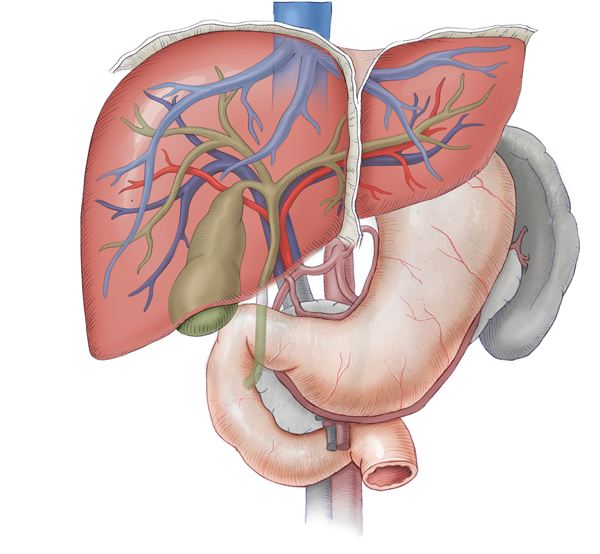
Einteilung
Bei den malignen Lebertumoren kann man primär von der Leber ausgehende Karzinome der Leberzellen oder der Gallengänge von sekundären Formen abgrenzen, die am häufigsten Absiedelungen von kolorektalen Karzinomen sind. Beim kolorektalen Karzinom bedeutet eine Fernmetastasierung im Übrigen nicht, dass eine kurative Resektion nicht mehr möglich ist. In solchen Fällen ist entscheidend, dass nach einer - eventuell auch ausgedehnten Leberresektion - genug gesundes Lebergewebe übrig bleibt. Gleiches gilt auch für Metastasen in der Lunge.
Hepatozelluläres Karzinom
Das hepatozelluläre Karzinom ist der weltweit am häufigsten vorkommende solide Tumor und ist mit 85% der soliden Lebertumore im Vergleich wesentlich häufiger als das cholangiocellulären Karzinom, das etwa 15% der von der Leber ausgehenden Karzinome ausmacht.
Ätiologie
Die Häufigkeit des HCC ist dabei regional stark unterschiedlich. In Gebiete Südchinas, Südafrikas und in Taiwan gilt es als endemisch. Dies liegt an der hohen Prävalenz chronischer viraler Hepatitiden in diesen Ländern. Die Virushepatitis ist ein wesentlicher Risikofaktor für die Entstehung eines HCC. Dies erklärt auch, warum durch die Impfung gegen Hepatitis B und die dadurch erreichte Senkung der Hepatitis-B-Prävalenz von 15% auf 1% die Entstehungsrate eines HCC dramatisch gesenkt werden konnte. 1,2
Noch wichtiger in der Entstehung solcher Karzinome ist das Vorliegen einer Leberzirrhose, sei sie nun viral oder äthyltoxisch bedingt. Andere Faktoren wie das Kanzerogen Aflatoxin oder seltene Eisenspeicherkrankheiten wie die Hämochromatose spielen eine eher untergeordnete Rolle.
In Deutschland liegt die Inzidenz bei ca. 5/100.000 Einwohner pro Jahr. Da als Ursache bei uns hauptsächlich eine Leberzirrhose zu finden ist, macht es durchaus Sinn, Risikopatienten in Bezug auf die Entstehung eines HCC zu überwachen. Allerdings ist eine solche Surveillance nur dann sinnvoll, wenn auch eine Therapieoption zur Verfügung steht. Ein Patient mit einer Leberzirrhose CHILD C ohne Chance auf eine Transplantation muss auch nicht regelmäßig kontrolliert werden, da auch das Risiko für eine Resektion eines HCC zu groß wäre. Zur Überwachung, die alle 6 Monate erfolgen sollte, eignet sich der sehr spezifische Tumormarker AFP, der im Gegensatz zu vielen anderen Tumormarkern auch als Screeningparameter eingesetzt werden kann. Zusätzlich wird eine Sonografie des Abdomens durchgeführt. 3
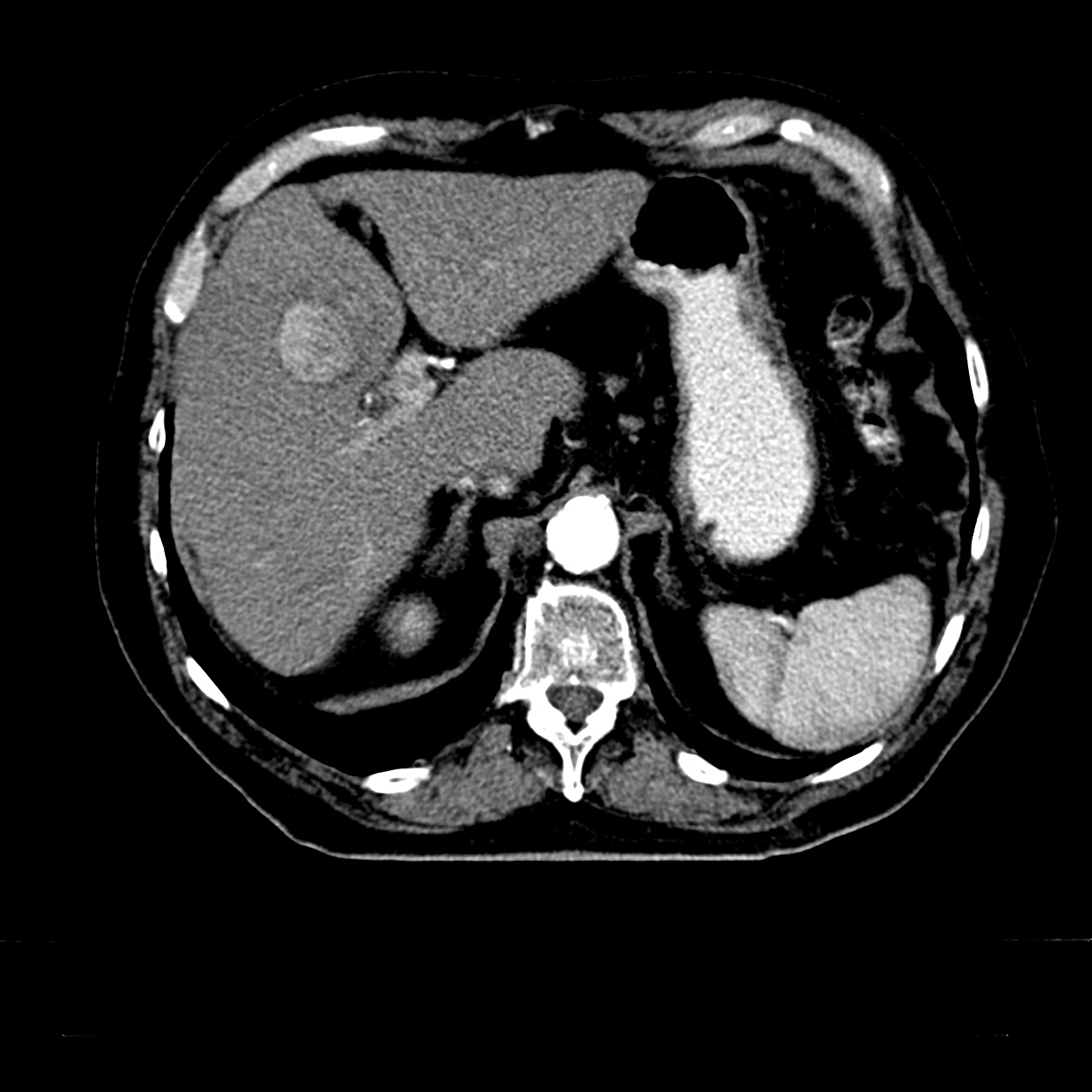
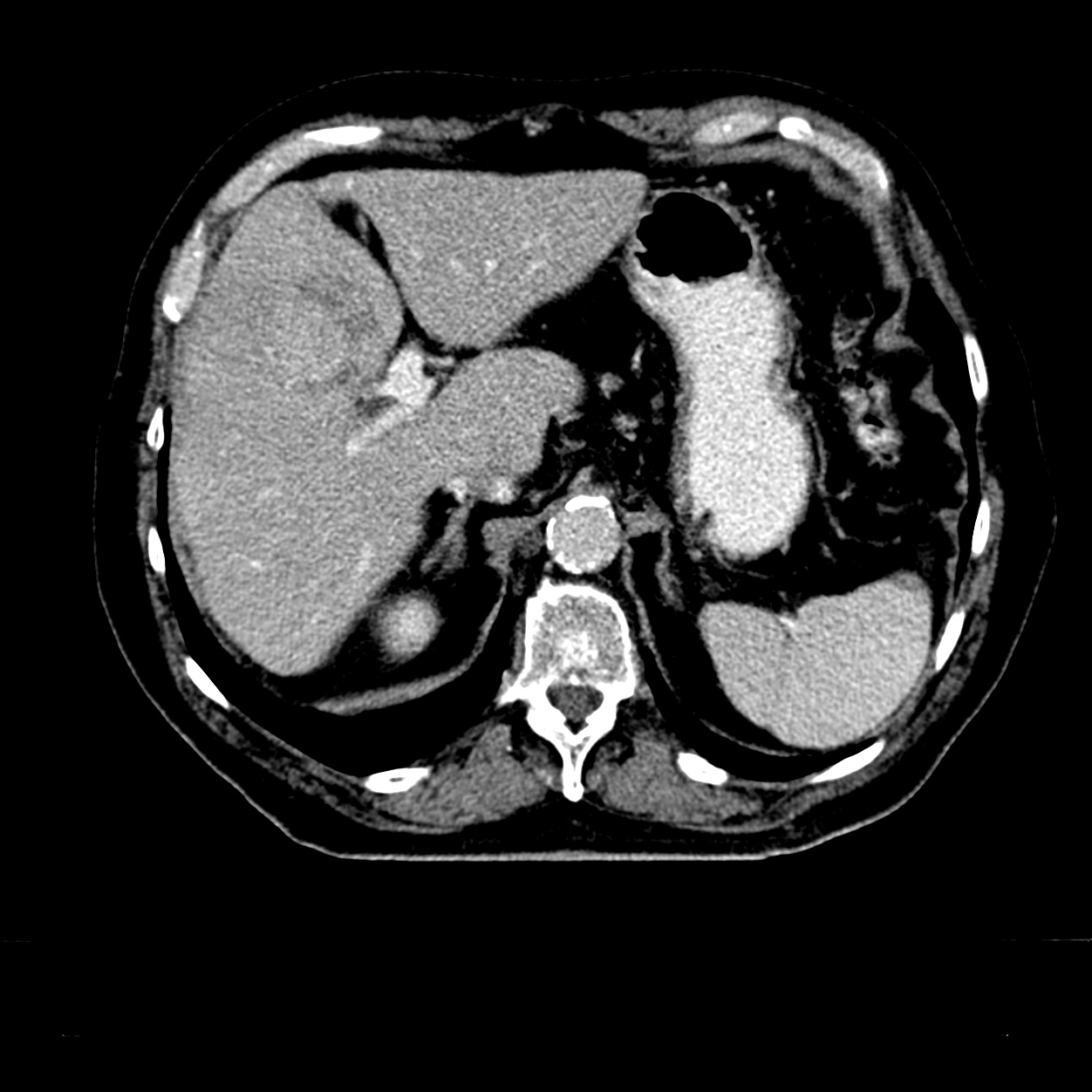
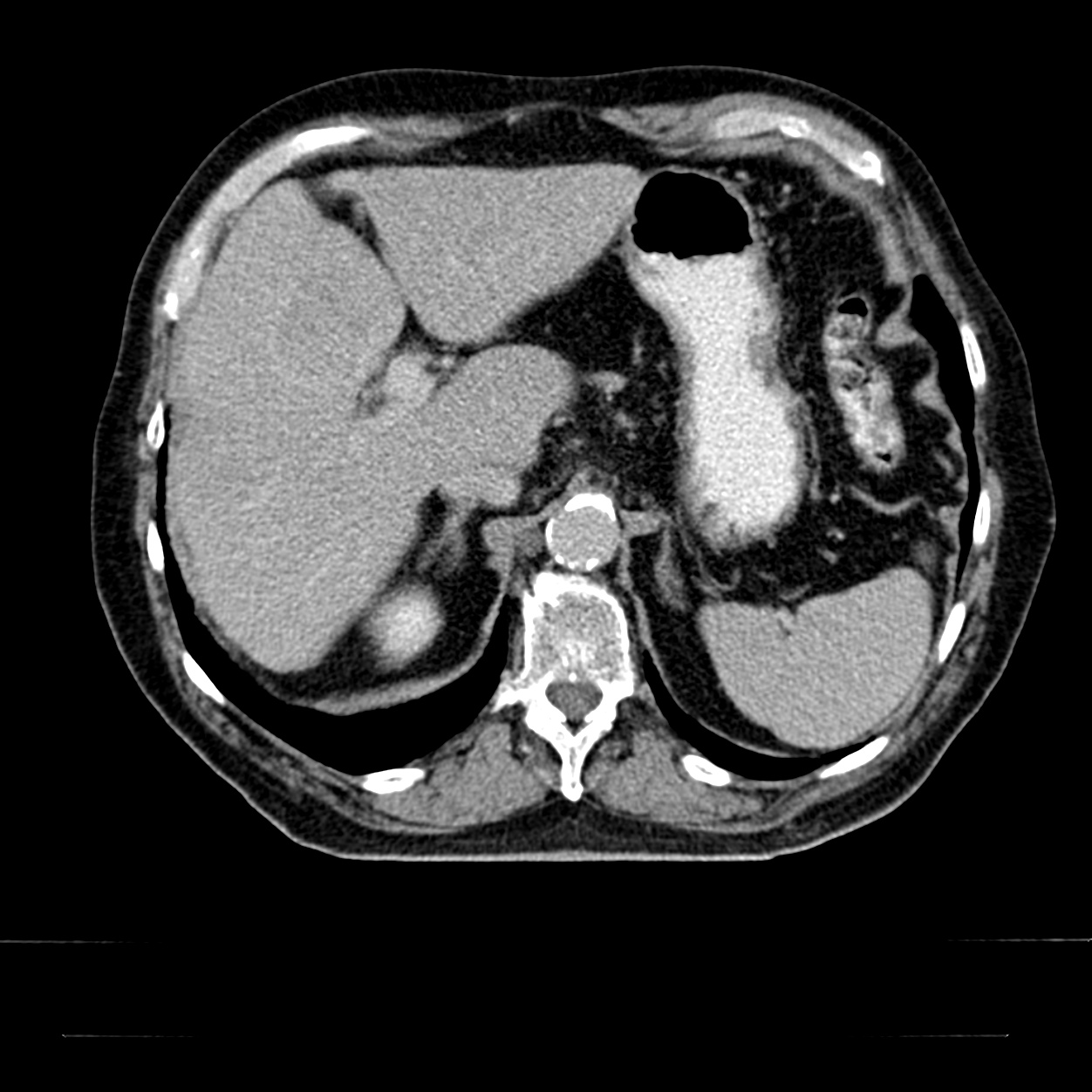
Patientenbeispiel HCC
Hier sehen Sie das CT eines Patienten mit einem HCC im Seg. 4b der Leber. Durch das spezifische Kontrasmittelverhalten im Dreiphasen-CT kann die Verdachtsdiagnose erhärtet werden. Wenn gleichzeitig das AFP signifikant erhöht ist, ist die Diagnose des HCC gesichert.
Therapie
Die Therapie des HCC besteht aus Resektion des Befundes, einer Lebertransplantation oder lokal Ablativen Verfahren. Diese kommen dann zum Einsatz, wenn ein Befund nicht resektabel sein sollte, der Patient nicht operationsfähig ist oder die Zeit bis zu einer Lebertransplantation überbrückt werden muss, ohne dass die Tumore größer werden oder neue hinzu kommen.
Die Lebertransplantation stellt beim HCC tatsächlich eine Therapieoption dar. Dies ist eine Besonderheit dieses Tumors, in der Tat ist eine Karzinomerkrankung ja ansonsten eher ein Ausschlusskriterium für eine Transplantation. Die Indikation zur Transplantation wird dabei anhand der sog. Milan-Kriterien gestellt. Nach diesen sollte ein solitärer HCC-Herd nicht größer als 5 cm sein. Liegen mehrere Herde vor, so dürfen es nicht mehr als drei und diese nicht größer als 3 cm sein.
Die entscheidende Frage, die sich bei einer Leberresektion stellt, ist, wieviel funktionell intaktes Restgewebe nach der Resektion verbleibt. Das reine Volumen lässt sich sehr gut mit einer CT-Volumetrie abschätzen. Allerdings sind Volumen und Funktion nicht gleichzusetzen, insbesondere bei eingeschränkter Leberfunktion, beispielsweise durch eine Fibrose oder Zirrhose der Leber. Die Funktion der Leber kann man besser in Leberfunktionstests wie dem LIMAX abschätzen.
Zwar ist es so, dass sich die Leber sehr rasch regenerieren kann und der verbleibende Rest innerhalb von ein paar Monaten auf annähernd normale Lebergröße hypertrophiert. Entscheidend ist aber die unmittelbare Phase nach der Operation, in der ein Leberversagen droht, wenn dieser Rest funktionell zu klein ist.
Ist eine ausgedehnte Resektion der Leber erforderlich, bei der das vermutlich verbleibende Restvolumen unter 25 % ist, kann man sich die Hypertrophieeigenschaft der Leber auch insofern zu Nutze machen, als dass man sie gezielt induziert. Hierfür ist es wichtig zu verstehen, dass die Leber nicht ausschließlich arteriell mit Sauerstoff versorgt wird. Bis zu 80% der Sauerstoffversorgung der Leber erfolgt über den portalvenösen Kreislauf, der einen sehr hohen Blutfluss aufweist.
Verschließt man einen Pfortaderast, ist dies ein starker Hypertrophiereiz für die Gegenseite der Leber. Dieser Verschluss kann entweder interventionell radiologisch erfolgen mittels Pfortaderembolisation oder operativ. Dies erfolgt beispielsweise im Rahmen einer atypischen Resektion auf der linken Seite der Leber, bei der im zweiten Schritt eine Hemihepatektomie durchgeführt werden soll. Ligiert man nun bei dieser ersten Operation den rechten Pfortaderast, wird dieser Teil der Leber zwar nicht nekrotisch, aber hypoxisch und in seiner Funktion herabgesetzt. Der weiterhin voll perufundierte linke Teil der Leber hypertrophiert sehr stark, so dass nach einigen Wochen eine ausgedehnte Resektion möglich wird, ohne Gefahr zu laufen, ein Leberversagen zu verursachen.
Eine Weiterentwicklung dieser zweizeitigen Resektion ist ein sog. In-Situ-Split der Leber. Hierbei wird nicht nur der Pfortaderast der später zu resezierenden Leberhälfte ligiert, sondern bereits das komplette Parenchym der Leber in der späteren Resektionsgrenze durchtrennt. Da dadurch intrahepatische Kollateralen unterbunden werden, verstärkt und beschleunigt dies die Hypertrophie der Leber, so dass bereits nach wenigen Tagen die zweite OP erfolgen kann. So läuft man nicht Gefahr, dass ein Metastasengeschehen während der Hypertrophiephase voranschreitet.
Lokal ablative Verfahren
Besteht keine funktionell sinnvolle Möglichkeit der Resektion, oder sollen HCC-Herde bis zu einer möglichen Lebetransplantation konstant und lokal unter Kontrolle gehalten werden, kommen lokal ablative Maßnahmen zum Zuge. Hierbei ist eine gezielte transarterielle Chemoembolisation(TACE) möglich, bei dem ein HCC-Herd superselektiv mittels Angiografie dargestellt wird. Dann wird über die nur den Herd versorgende Arterie ein Chemotherapeutikum instilliert und das Gefäß anschließend verschlossen. Dies setzt natürlich einen gut und über ein exclusives Gefäß vaskularisierten Befund voraus. Dies ist vor allem beim HCC der Fall. Bei kolorektalen Lebermetastasen ist eine TACE in der Regel nicht sinnvoll. Hier kommt eher die Radiofrequenzablation RFA zum Einsatz. Hierbei wird die Metastase percutan oder intraoperativ über eingestochene Nadeln mit Radiofrequenzstrom verödetet.
Cholangiocelluläres Karzinom
Im Vergleich zum hepatocellulären Karzinom ist das CCC bei uns deutlich seltener. Anhand der Lokalisation kann man zwischen Gallenblasenkarzinom, intrahepatischen Gallengangskarzinomen, zentralen und distalen Gallengangskarzinomen unterscheiden. Die zentralen Gallengangskarzinome werden auch als Klatskin-Tumore bezeichnet und nach der Bismuth-Klassifikation weiter unterteilt.1
Die Therapie bzw. die operative Strategie unterscheidet sich je nach Lokalisation ganz wesentlich. Ein intrahepatisches Gallengangskarzinom wird mittels Leberresektion der betroffenen Segmente behandelt. Ein Gallenblasenkarzinom mit Cholezystektomie mit Lebersegment- und ggf. Gallengangsresektion.
Ein Klatskin-Tumor je nach Ausbreitung mit Hemihepatektomie rechts oder links bzw. einer distalen Gallengangsresektion. 2
Distale Gallengangskarzinome werden ähnlich wie ein Pankreaskopfkarzinom mit einer partiellen Duodenopankreatektomie behandelt. Die klassische Variante dieser OP mit Resektion des Magenantrum enstpricht der Whipple’schen Operation, ansonsten spricht man von einer Operation nach Traverso-Longmire
Die Lebertransplantation spielt als Therapieoption beim zentralen CCC momentan keine Rolle, könnte aber in Zukunft wieder an Bedeutung gewinnen. Aktuelle Studien zu diesem Thema untersuchen dies.
Literatur:
- ADENOCARCINOMA OF THE HEPATIC DUCT AT ITS BIFURCATION WITHIN THE PORTA HEPATIS. AN UNUSUAL TUMOR WITH DISTINCTIVE CLINICAL AND PATHOLOGICAL FEATURES.
Am J Med. 1965 Feb;38:241-56.: KLATSKIN G. - Management strategies in resection for hilar cholangiocarcinoma.Ann Surg. 1992 Jan;215(1):31-8.: Bismuth H1, Nakache R, Diamond T.

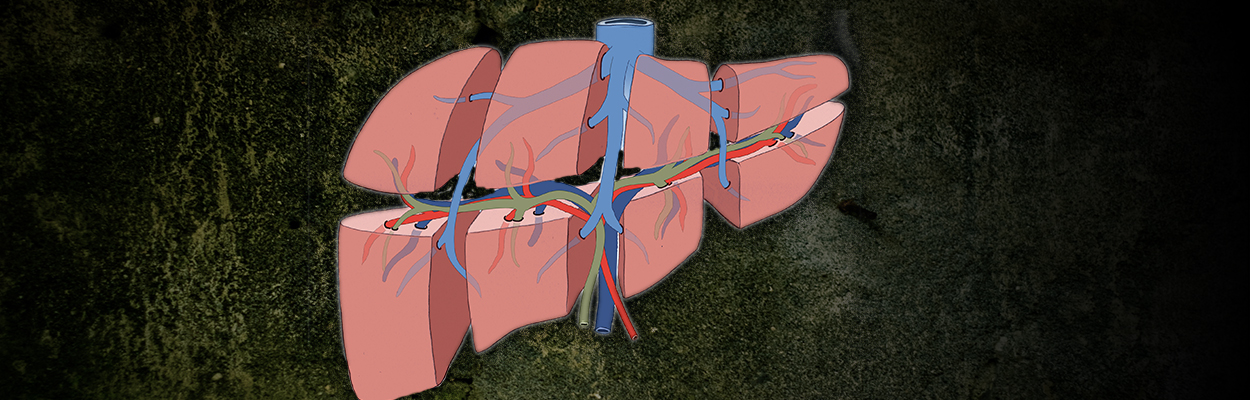
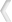
 Wunde, Wundheilung
Wunde, Wundheilung Infektion
Infektion Akutes Abdomen
Akutes Abdomen Abdominaltrauma
Abdominaltrauma Ileus
Ileus Hernien
Hernien Struma benigna
Struma benigna Schilddrüsen-CA
Schilddrüsen-CA Nebenschilddrüsen
Nebenschilddrüsen Hypderthyreose
Hypderthyreose Nebenniere
Nebenniere Achalasie
Achalasie Ösophagus-CA
Ösophagus-CA Ösophagusdivertikel
Ösophagusdivertikel Ösophagusperforation
Ösophagusperforation Verätzung
Verätzung Magen-CA
Magen-CA Ulkuskrankheit
Ulkuskrankheit GERD
GERD Adipositas
Adipositas CED
CED Divertikulitis
Divertikulitis Kolon-CA
Kolon-CA Proktologie
Proktologie Rektum-CA
Rektum-CA Anatomie
Anatomie Ikterus
Ikterus Cholezystolithiais
Cholezystolithiais Benigne Leberläsionen
Benigne Leberläsionen Maligne Leberläsionen
Maligne Leberläsionen Pankreatitis
Pankreatitis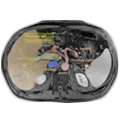 Pankreaskarzinom
Pankreaskarzinom