Tiefe Venenthrombose (TVT), Thrombophlebitis superficialis und Phlegmasia coerulea dolens
Tiefe Venenthrombose
Als „Thrombose“ bezeichnet man den vollständigen oder teilweisen Verschluss von Arterien oder Venen sowie der Herzhöhlen durch intravasale Blutgerinnung mit Bildung von Blutkoageln aus Thrombozytenaggregaten und Fibrin (Pschyrembel 259. Auflage S. 1656).
Pathophysiologie
Die Pathophysiologie der Thrombose wird im Wesentlichen durch die „Virchow-Trias“ beschrieben: 1. Gefäßwandschaden (z.B. durch Entzündung, Arteriosklerose und Trauma), 2. Stase und verminderte Blutzirkulation (z.B. im Rahmen einer Fraktur-Ruhigstellung durch Gips), 3. Veränderte Blutzusammensetzung / Hyperkoagulabilität (z.B. im Rahmen von angeborenen Gerinnungsstörungen oder z.B. beim exsikkierten Patienten).
Vorkommen / Risikokollektiv
Die Thrombose kommt gehäuft bei Patienten mit angeborenem Protein-C- und Protein-S-Mangel, APC-Resistenz oder Antithrombin-III-Mangel, bei Frauen >40Jahre, bestehender Varikose, Adipositas, hormonellen Veränderungen (Kontrazeptiva, Schwangerschaft, Cushing-Syndrom), Diabetes mellitus, Vena-cava-inferior-Syndrom, Polytrauma und nach längeren Operationen sowie als paraneoplastisches Syndrom bei Tumorerkrankungen vor (Pschyrembel 259. Auflage S. 1656).
Klinik
Klinisch besteht eine überwärmte, livide geschwollene, umfangsvermehrte Extremität. Gelegentlich können Umgehungskreisläufe beobachtet werden (sog. „Pratt-Warnvenen“) oder eine Glanzhaut vorliegen. Unspezifische Allgemeinsymptome (Fieber, Leukozytose, Tachykardie) können ebenfalls auftreten.
Komplikationen
Die Hauptkomplikationen einer TVT bestehen in Ascension des Thrombus, der pulmonalen Embolisation (Lungenembolie) und der Entwicklung des Postthrombotischen Syndromes (PTS), einem pathologischen Residualzustand nach Defektheilung mit zerstörtem Klappenapparat und Entwicklung des klinischen Bildes der Chronisch Venösen Insuffizienz (CVI).
Diagnostik
Die typischen, oftmals beschriebenen klinischen Tests auf Vorliegen einer Thrombose sind oftmals unspezifisch, ungenau und stark untersucherabhängig.
Wells-Score
Aus gezielter Anamnese und klinischer Untersuchung sollte der sogenannte Wells-Score ermittelt werden, der zur Abschätzung der klinischen Wahrscheinlichkeit einer Thrombose dient und das weitere Vorgehen mitbestimmt. Ein Score-Wert >2 lässt demnach eine Thrombose klinisch wahrscheinlich erscheinen und weitere Massnahmen veranlassen.

Tabelle entnommen aus:
S2k-Leitlinie zur Diagnostik und Therapie der Venenthrombose und der Lungenembolie
| Klinische Charakteristik | Score |
|---|---|
| Aktive Tumorerkrankung | 1 |
| Lähmung oder kürzlich Immobilisation der Beine | 1 |
| Bettruhe(> 3 Tage); große Chirurgie (< 12 Wochen) | 1 |
| Schmerz/Verhärtung entlang der tiefen Venen | 1 |
| Unterschenkelschwellung > 3 cm gegenüber der Gegenseite | 1 |
| Eindrückbares Ödem am symptomatischen Bein | 1 |
| Kollateralvenen | 1 |
| Frühere dokumentierte TVT | 1 |
| Alternative Diagnose mind. ebenso wahrscheinlich wie TVT | -2 |
Wells-Score Tabelle 1 (AWMF-Leitlinie, Pocket-Version)
D-Dimere
Weiteren Aufschluss können auch die Bestimmung der D-Dimere im Blut geben. Als Fibrinspaltprodukte können sie bei einer TVT vermehrt anfallen und erhöht sein, wie allerdings in multiplen anderen Situationen auch (z.B. bei Z.n. Operation oder Entbindung). Die D-Dimere haben die höchste Aussagekraft, wenn sie nicht erhöht sind. Ist dann die klinische Wahrscheinlichkeit nach dem Wells-Score noch gering, muss nichts weiter veranlasst werden (hoher negativer prädiktiver Wert). Zudem bieten sich die D-Dimere zur Verlaufskontrolle nach mehrmonatiger Therapie an.
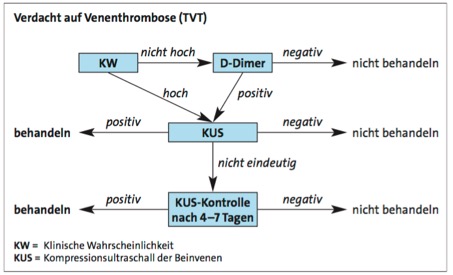
Den gesamten Untersuchungsalgorithmus zeigt Abb. 1 aus der Leitlinie (AWMF, Pocketversion):
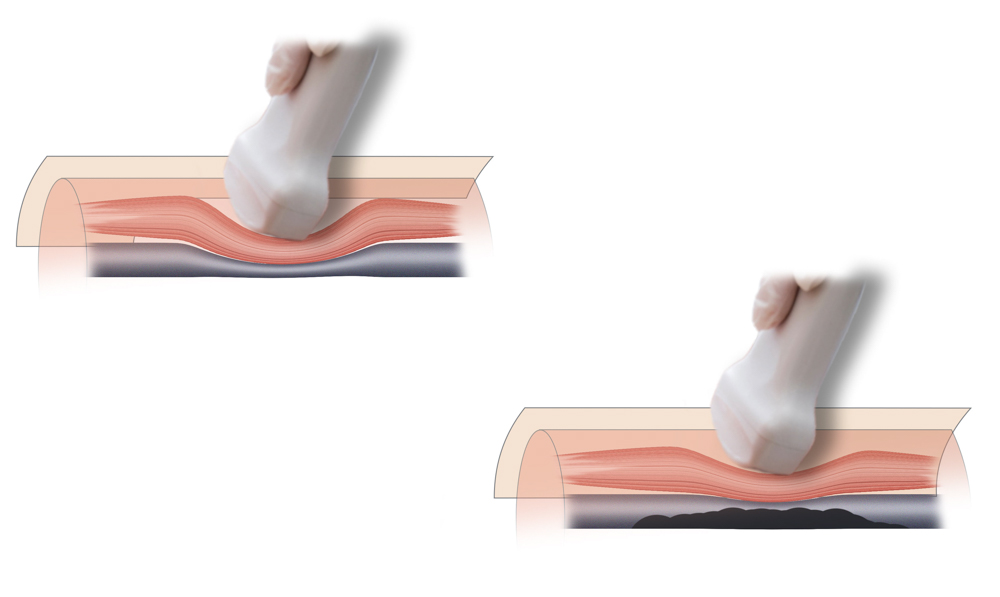
FKDS
Den Goldstandard der Diagnostik bei hoher klinischer Wahrscheinlichkeit nach Wells stellt die FKDS (farbkodierte Duplexsonographie) dar. Liegend sollte das gesamte tiefe Venensystem des Beines (VF, Vpop, Vv. fib., Vv. tib. post., Vv. tib. ant., die Muskelvenen von M. gastrocnemius und M. soleus) im Querschnitt im sogenannten B-Mode (brightness mode) in 1-2cm Abständen komprimiert werden. Zudem kann mit verstärktem Dopplersignal im Längsschnitt Spontanfluss und Atemmodulierbarkeit der Vene untersucht werden. Insbesondere die Untersuchung der Unterschenkelvenen kann schwierig sein. Poplitealvene und Unterschenkelvenen können oftmals im Sitzen besser untersucht werden.
Auch das oberflächliche Venensystem (VSM, VSP, Crossen) gilt es zu untersuchen, um keine Thrombophlebitis oder Crossenascension zu übersehen.
MR- oder CT-Phlebographien können im Einzelfall zusätzlich bei der Diagnosestellung helfen. Immer sollte an eine onkologische Grunderkrankung gedacht werden und die Diagnostik ggf. um Abdomen-CT, Gastroskopie, Koloskopie, Gyn-Konsil etc. ergänzt werden.
Eine initiale, laborchemische Thrombophiliediagnostik ist ohne Stellenwert!
Therapie
Die Therapie der TVT ist primär konservativ und besteht aus den Bausteinen Kompression, Mobilisation und Antikoagulation. Ziele sind die Verhinderung von Thrombusascension, -Embolisation und Postthrombotischem Syndrom.
Kompression
Bis ein geeigneter Kompressionstrumpf der KKL II vorhanden ist, empfiehlt sich die Wickelung des Beins, idealerweise z.B. mit einem 2-Komponenten-Kompressionssystem (z.B. Urgo-K2-Bandagen). Cave: Fusspulse !? ABI>0,8?).
Mobilisation
Der Patient sollte mobilisiert werden, eine Immobilisation ist kontraindiziert! Nur im Ausnahmefall, z.B. bei starker Schwellung, sollte das Bein intermittierend hochgelagert werden.
Antikoagulation
Bei Diagnosestellung sollte umgehend mit einer therapeutischen Antikoagulation begonnen werden. Hier bietet sich eine überlappende Vollantikoagulation mit niedermolekularem Heparin (NMH) mit umgehender, anschliessender Marcumarisierung an. Alternativ stehen die sog. NOAKs zur Verfügung (z.B. Rivaroxaban, Apixaban,...). Sie müssen laborchemisch nicht „gemonitort“ werden und benötigen kein „Bridgeing“ mit NMH. Die einzelnen Substanzen und Dosierungen können an dieser Stelle am besten der AWMF-Leitlinie entnommen werden.
Länge der Antikoagulation
Die „Gretchen-Frage“ in der TVT-Behandlung ist die Frage nach der Behandlungsdauer. Man unterscheidet generell eine Initialtherapie (IT), Erhaltungstherapie (ET, 3-6 Monate) und eine Verlängerte Erhaltungstherapie (VET, >6 Monate). Welcher Patient die letztere benötigt, ist Gegenstand ständiger Diskussion. Hier spielen unten angebene Faktoren eine Rolle.
Mittlerweile werden auch NOAKs in reduzierter Dosis als VET diskutiert. Im Regelfall wird eine TVT zunächst einmal 3-6 Monate antikoaguliert. Eine Unterschenkelvenenthrombose sollte generell nicht länger als 3 Monate therapiert werden, auch wenn es sich um ein Rezidiv handelt oder eine idiopathische Thrombose vorliegt.
| Kriterium | Für fortgesetzte Therapie |
Gegen fortgesetzte Therapie |
|---|---|---|
| Risikofaktor | fortbestehend | passager |
| Genese | unklar | getigert |
| Rezidiv | ja | nein |
| Bisherige Antikoagulationsqualität | gut | schlecht |
| D-Dimere (nach Therapieende) | erhöht | normal |
| Residualtrhombus | vorhanden | fehlend |
| Geschlecht | männlich | weiblich |
| Thrombusausdehnung | langstreckig | kurzstreckig |
| Thrombuslokalisation | proximal | distal |
| Schwere Thrombophilie | ja* | nein** |
| Patientenpräferenz | dafür | dagegen |
* z.B. Antiphospholipipdsyndrom
** z.B. heterozygote Faktor V- oder heterozygote Prothrombin-Mutation
Die Kriterien für eine verlängerte Erhaltungstherapie (AWMF-Leitlinie, Pocket-Version)
Interventionell / operative Therapie
Gerade im Hinblick auf die Entwicklung eines Postthrombotischen Syndromes beim jungen Patienten mit erheblicher Invalidität neigen einige Kliniken dazu, analog zur Praxis im amerikanischen Sprachraum, insbesondere ilio-femorale Thrombosen frühzeitig zu rekanalisieren. Hier stehen Fibrinolytika (systemisch oder kathetergestützt), Thrombektomiemanöver und iliakale Venen-Stent-Applikationen zum Beispiel bei Vorliegen eines Beckenvenensporns / May-Turner-Syndroms (narbig-sklerotische Intimaproliferation durch pulssynchrone Einklemmung der linken Vena iliaca communis zwischen Arteria iliaca communis rechts und Lendenwirbel) zur Verfügung. Hier „scheiden sich die Geister“: Studien belegen bislang keine Vorteile.
Thrombose in der Schwangerschaft
In der Schwangerschaft besteht ein 4x erhöhtes TVT-Risiko. Eine Bestimmung der D-dimere macht keinen Sinn, es sollte direkt ein Kompressionsultraschall bei klinischem Verdacht durchgeführt werden.
Die Therapie besteht aus Kompression und Vollantikoagulation mit NMH, Vitamin-K-Antagonisten und Marcumar sind kontraindiziert. In der Stillzeit kann Warfarin verabreicht werden, ebenso eignet sich z.B. Orgaran.
Thrombophlebitis superficialis
Die oberflächlichen Venenthrombosen von VSM und VSP dürfen im Hinblick auf ihre klinische Bedeutung und auch das pulmonale Embolisationsrisiko nicht unterschätzt werden.
Astvarizen werden mit NSAR behandelt, Thrombophlebitiden in der VSM > 5cm Thrombuslänge werden für 4-6 Wochen mit niedermolekularem Heparin low dose behandelt (z.B. Arixtra) unter regelmäßigen Ultraschallkontrollen zum Ausschluss einer Ascension.
Reicht die Thrombophlebitis <3cm an die Crosse heran, wird die Oberflächenthrombose wie eine tiefe Beinvenenthrombose behandelt. Bei Crossenbeteiligung führen viele Kliniken noch eine Notfall-Crossektomie mit Extraktion des in die Crosse hineinragenden Thrombusmaterials durch. Dieses Vorgehen wird diskutiert und von einigen nicht mehr als notwendig erachtet.
Notfall Phlegmasia coerulea dolens
Bei der Phlegmasia coerulea dolens handelt es sich um eine Thrombosierung der gesamten venösen Ausflussbahn. Der venöse „Querschnittsverschluss“ führt zur Kompromittierung auch der arteriellen Perfusion.
Klinisch besteht eine massive Schwellung, Schmerzen, eine zyanotische Extremität, ggf. Spannungsblasen, ein (drohendes) Kompartment und eine Schocksymptomatik bei hohem Flüssigkeitsverlust.
In ca. 30% der Fälle liegt eine maligne Grunderkrankung zugrunde, in 30% zudem eine Lungenembolie. Die Letalität beträgt bis zu 50%.
Die Phlegmasie ist insgesamt ein hochdramatisches Krankheitsbild, Extremität und Patient sind akut vital bedroht.
Die Therapie besteht in der sofortigen, notfallmäßigen venösen Rekanalisation i.e.L. durch eine venöse Thrombektomie. Als „bail-out-Proceduren“ kommen als ultima ratio venöse Bypassierungen in Betracht (z.B. Transposition der gegenseitigen Vena saphena magna im Rahmen einer Palma-OP), um den dringend erforderlichen venösen Abstrom zu gewährleisten.
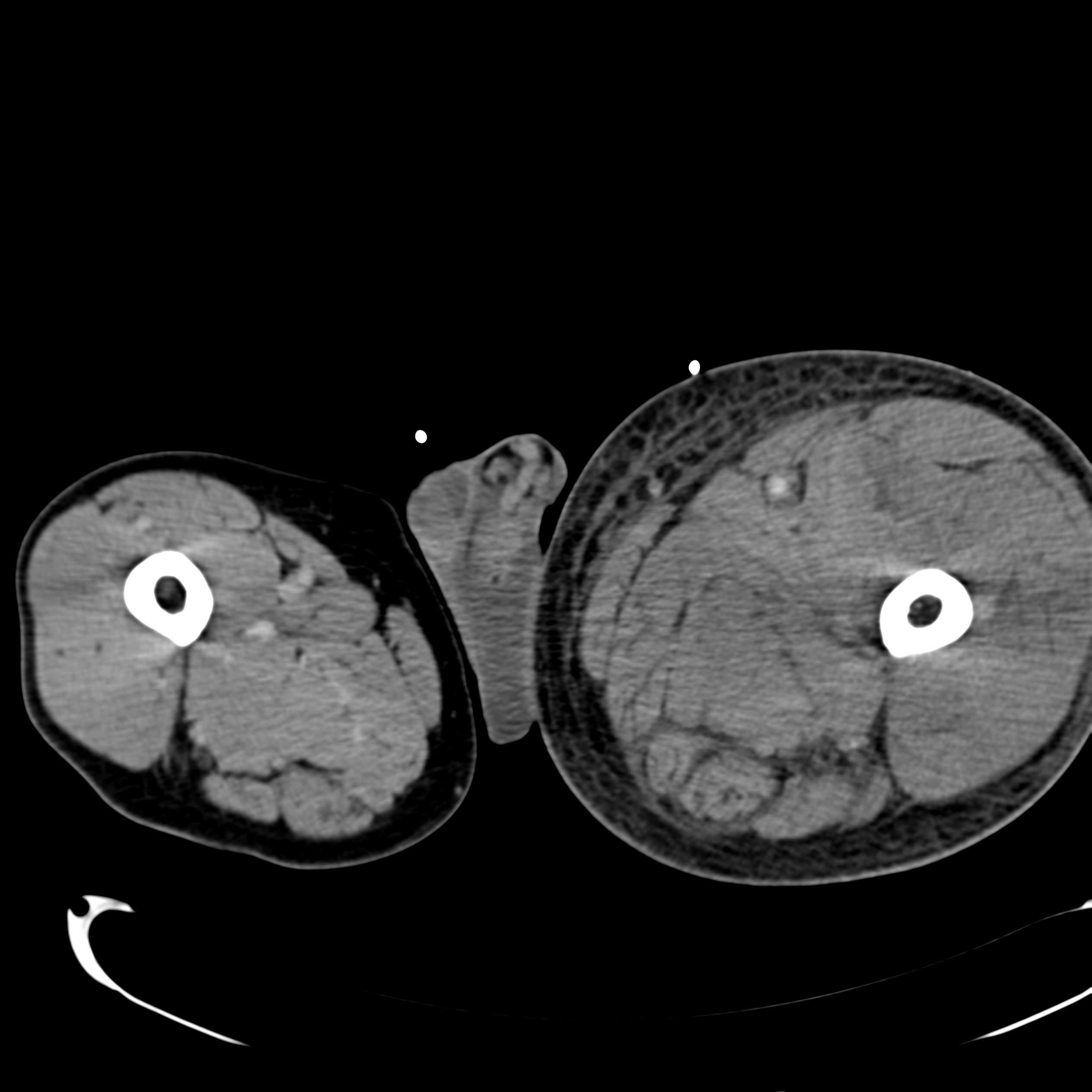
CT einer Phlegmasia coerulea dolens
